Saul Hertz y los usos del yodo en radiomedicina
Otorgado al Hospital General de Massachusetts, en Boston, el 8 de octubre de 2021.
En Boston, un día de la primavera de 1941, un joven doctor del Hospital General de Massachusetts (MGH, por sus siglas en inglés) quedó a tomar una copa con una mujer. Aunque parezca una cita, el ambiente era totalmente diferente y nada relajado. El doctor Saul Hertz le había preparado un cóctel "atómico" a Elizabeth D, una paciente con síntomas de hipertiroidismo. Con la esperanza de curar sus dolencias, ella ingirió valientemente un cóctel de yodo radiactivo, producido por el Instituto Tecnológico de Massachusetts (MIT, por sus siglas en inglés).
Esta cita unió para siempre a la física de partículas y la medicina clínica. Juntas, engendraron un nuevo campo: la medicina nuclear. Gracias a los descubrimientos de Hertz y otros investigadores, a día de hoy utilizamos yodo radiactivo y otros medicamentos radiactivos de forma rutinaria para el diagnóstico y tratamiento de enfermedades, para mejorar y salvar las vidas de millones de personas.
Contenidos
Una pregunta esencial
La relación floreciente entre medicina y física había empezado unos años antes, poco después de que Frédéric Joliot y Irène Joliot-Curie recibieran el premio Nobel de Química en 1935. Este premio reconocía su labor sintetizando nuevos isótopos radiactivos artificiales. El 12 de noviembre de 1936, el presidente del MIT dio una charla en la Escuela de Medicina de la Universidad de Harvard titulada: "Qué puede hacer la física por la biología y la medicina". En esta ocasión, mencionó la posibilidad de fabricar isótopos radiactivos para buscar nuevas aplicaciones en medicina.
Hertz, entonces director de la clínica de tiroides en el MGH, asistió a la charla. También acudieron otros médicos, como el Dr. James Howard Means, jefe médico del MGH y uno de los pioneros de la clínica. Hertz era endocrino y especialista en tiroides. Esta glándula con forma de mariposa y recubierta de bultitos había cautivado a Hertz, que estudiaba maravillado cómo regula el metabolismo con la precisión de un reloj suizo. Hasta que deja de funcionar. Por ello, dedicaba sus horas de trabajo a arreglar tiroides defectuosas, una condición que suele afectar más a las mujeres, y que incluye problemas como la pérdida de peso, la fatiga, la ansiedad y la irritabilidad.
Una tiroides "hiperactiva" puede extirparse mediante cirugía. Sin embargo, en algunos pacientes con enfermedad de Graves (una enfermedad autoinmune que causa hipertoidismo), este procedimiento es muy costoso y peligroso. Por este motivo, tanto Hertz como Means buscaban una alternativa. Probaron a bombardear a los pacientes con rayos X para destruir el tejido dañado, pero era una solución problemática: la radiación también dañaba los tejidos sanos.
Varios estudios habían establecido que la tiroides absorbe yodo, necesita este elemento para funcionar correctamente. La falta de yodo causa una enfermedad: el bocio. Durante la charla de Compton, algo hizo clic en la cabeza de Hertz. Levantó la mano y preguntó algo esencial: "¿Podría fabricarse yodo radiactivo, de forma artificial?"
La respuesta llegó al cabo de un mes. Compton confirmó las sospechas de Hertz; unos años atrás, en 1934, el físico Enrico Fermi había fabricado yodo radiactivo. Los resultados estaban publicados en la revista científica Nature. Este isótopo artificial de yodo (el yodo-128) tiene una semivida de 25 minutos. En ese tiempo, la mitad de los átomos de yodo radiactivo en una muestra se han desintegrado. Durante este proceso, los átomos emiten radiación. La mitad del yodo-128 remanente seguirá transmutando y emitiendo radiación, hasta que no queden restos de la sustancia radiactiva.
Hertz aventuró que quizás la desintegración radiactiva del yodo-128 podría eliminar el tejido "hiperactivo" de la tiroides. Pero, al contrario que los rayos X, dejaría inalterado al tejido sano, porque el yodo es absorbido de forma muy selectiva por esta glándula. El 23 de diciembre de 1936, escribió una carta a Compton: "[espero que el yodo radiactivo] sea un método terapéutico útil para tratar los casos de tiroides hiperactivo."
Hertz no perdió tiempo y decidió investigar nuevos tratamientos. Junto con un colega investigador del MIT, un físico y reconocido pianista llamado Arthur Roberts, empezó a explorar la terapia con conejos. En 1937 consiguieron financiación de Harvard y decidieron inyectar estos animales con pequeñas cantidades de yodo-128. Roberts había usado una fuente de neutrones de radio y berilio para crear el yodo radiactivo artificial en el centro de radiactividad del MIT, liderado por Robley Evans.
Los investigadores midieron las emisiones radiactivas utilizando un contador Geiger. Según estas estimaciones, la mayor parte del yodo era absorbido por la tiroides, mientras que el resto se eliminaba con la orina. Buenas noticias: el yodo radiactivo no se acumula en ningún otro órgano. Y, todavía mejor, todo parecía indicar que la tiroides hiperactiva absorbía mucho más yodo que una glándula sana. Los estudios de Hertz y Roberts también demostraron que la radiactividad podía utilizarse para seguir los movimientos del yodo por el cuerpo y comprender mejor la fisiología de la tiroides. Pronto, predijo Hertz, el yodo radiactivo podría curar el bocio, las tiroides hiperactivas, incluso el cáncer. Pero para poder utilizar este tratamiento en humanos, necesitaban un isótopo con una semivida más larga.
En ese momento, curar el cáncer con isótopos radiactivos sonaba a utopía. Pocos médicos consideraban el potencial terapéutico de las partículas beta, emitidas por los átomos radiactivos desintegrándose y convirtiéndose en sustancias más estables. Pero Hertz no era el único científico avanzado a su tiempo.

"La selectividad de la tiroides para absorber el yodo que inyectamos en el cuerpo da muchas esperanzas. Si el yodo inyectado es radiactivo, podría convertirse en una terapia útil para tratar casos de hipertiroidismo."
— Saul Hertz en una carta al presidente del MIT, Karl Compton, escrita el 23 de diciembre de 1936
Primer estudio metabólico con yodo radiactivo en humanos
Casi al mismo tiempo que Hertz y Compton se encontraron en 1936, un médico e investigador de la Universidad de Yale, John Lawrence, estaba viajando a través de Estados Unidos en tren. Viajaba en tercera clase, era el único modo de poder transportar cientos de ratones de laboratorio. El joven doctor había recibido una invitación desde la Universidad de California Berkeley, donde trabajaba su hermano Ernest Lawrence. Unos años antes, Ernest había inventado uno de los aparatos más importantes para la física del siglo XX: un ciclotrón, una máquina para chocar átomos. Este descubrimiento le mereció el premio Nobel.
"Mi hermano y yo siempre habíamos pensado en la enorme oportunidad que supondría para la biología y la medicina usar técnicas propias de la física, la química y las matemáticas. Normalmente, las escuelas de medicina desdeñaban las ciencias básicas," recordaba John Lawrence durante una entrevista otorgada en 1979. Empezó a estudiar cómo el fósforo radiactivo creado por el ciclotrón podía curar la leucemia de sus ratones, concentrándose en las células de la médula ósea para aniquilar las células tumorales. Más tarde, probaría este tratamiento en pacientes humanos con leucemia. En 1939, utilizó este mismo método con éxito para tratar a pacientes con policitemia, una enfermedad que puede causar coágulos mortales.
Mientras tanto, Ernest había sugerido que John investigara otra cosa: debía encontrar otros médicos interesados en los usos de la radiactividad. "Queríamos utilizar [los isótopos radiactivos], tanto para terapia como para seguimiento de metabolitos," dice John.
Desafortunadamente, apenas encontró colaboradores. Uno de ellos fue el doctor Joseph Hamilton, un residente de medicina apasionado por la química, que venía de la Universidad de California San Francisco con la idea de utilizar el yodo radiactivo como trazador. Los trazadores permiten seguir los caminos metabólicos de diferentes sustancias en el cuerpo humano.
Para ellos, el tiempo también era un problema. Como Hertz y Roberts sabían, únicamente tenían acceso a yodo-128, cuya semivida solo permite estudios metabólicos en roedores y en conejos. No era un radioisótopo práctico para trabajar con humanos, porque se desintegra demasiado rápido para dar datos útiles.
En la primavera de 1938, Hamilton decidió buscar al hombre ideal para buscar nuevos trazadores radiactivos. Acorraló al químico Glenn Seaborg en el campus de la Universidad de California Berkeley. En una entrevista al Journal of Nuclear Medicine, Seaborg dijo: "Hamilton estaba estudiando el metabolismo de la tiroides con yodo-128, que tiene una semivida de 25 minutos. Se quejaba, fervientemente, de que esto fastidiaba sus planes." Entonces, Seaborg pidió a Hamilton concreción: ¿Qué necesitaba, exactamente? Contestó que un marcador radiactivo con una semivida de una semana sería ideal.
No tardó en tener buenas noticias. Seaborg y su colega John Livingood estaban trabajando sin descanso en el ciclotrón de Berkeley para fabricar el trazador perfecto. Para ello, bombardeaban átomos de teluro con deuterones (núcleos de deuterio, un isótopo del hidrógeno). El resultado fue un isótopo de yodo más estable: el yodo-131. Esta sustancia tenía una semivida de ocho días, cumpliendo con los requisitos de Hamilton a la perfección. También obtuvieron otros isótopos de yodo como el yodo-130, con una semivida de 12 horas.
John Lawrence decía que Hamilton era especialmente bueno convenciendo a la gente para participar en estudios clínicos. En este caso, tendría que persuadirles para beberse un cóctel de yodo-131 radiactivo fabricado en el ciclotrón de Berkeley. Hamilton llevó a cabo su estudio sobre el metabolismo del yodo en colaboración con Mayo Soley, un internista de la clínica de tiroides del Hospital de la Universidad de California San Francisco, que había estudiado anteriormente en el MGH. Como Hertz había descubierto con sus conejos el año anterior, el equipo californiano descubrió que la tiroides humana podía absorber yodo radiactivo.
"Es muy reconfortante saber que tanta gente está sana gracias a los avances científicos de gente como el doctor Hertz."
— La primera dama de EE.UU. Barbara Bush, que recibió tratamiento para una enfermedad de la tiroides, en una carta a la viuda de Hertz, Vitta Hertz
Primer tratamiento con yodo radiactivo en humanos
En Boston, el equipo del MIT y el MGH necesitaba su propia fuente de yodo radiactivo más longevo, y decidieron explorar la posibilidad de construir su propio ciclotrón. Por aquel entonces, las ayudas a la investigación provenían, mayoritariamente, de donaciones filantrópicas y fundaciones privadas, quienes elegían entre las diferentes propuestas de los científicos. En este caso, los investigadores lograron convencer a la Fundación Markle, en Nueva York, para que financiara un nuevo ciclotrón en el MIT.
El 31 de marzo de 1941, Hertz y Roberts tenían sus muestras de yodo radiactivo listas, gracias al ciclotrón Markle. Aunque casi todo era yodo-130, una pequeña cantidad de las muestras era yodo-131, el isótopo con semivida más larga.
Cuando Elizabeth D. se tomó el cóctel de yodo radiactivo y agua, se convirtió en la primera paciente en recibir este novedoso tratamiento para la tiroides. Roberts midió la absorción del radioisótopo con un contador Geiger, que situaba cerca del cuello de la paciente.
"La radioactividad era una cosa gloriosa, maravillosa," dijo Evans en una entrevista en 1978, donde también recuerda que antes de la Segunda Guerra Mundial apenas se temía a la radioactividad. Los pacientes se bebían "un vaso de agua con yodo radiactivo, y molaba. A los medios les encantaba. Al público, también."
Hertz siguió dando estos cócteles radiactivos a sus pacientes. Mientras tanto, en California, Hamilton, Soley y John Lawrence empezaron sus propios estudios terapéuticos en 1941. Ambos equipos estaban entusiasmados con los resultados: la hinchazón del bocio disminuía sin apenas complicaciones. Durante una conferencia en 1942, Hertz informó que el yodo radiactivo "va directamente a la tiroides inflamada y, en apenas 15 minutos, emite suficiente radiación como para convertirse en un tratamiento prometedor."
El concepto de "teragnósticos", sustancias que, al mismo tiempo, pueden utilizarse para diagnosticar y tratar una enfermedad, se convertiría en un éxito absoluto. La primera hipótesis de Hertz dio en el clavo.
En 1943, Hertz tuvo que abandonar temporalmente su clínica y su investigación para unirse a la armada estadounidense como voluntario, al mismo tiempo que avanzaba la medicina nuclear. Mientras tanto, Evans y Chapman continuaron el trabajo del equipo de la costa este en el MGH.
Después de la guerra, en 1946, los equipos de Boston y California presentaron los resultados de sus estudios, tras años de trabajos y varios pacientes. Las conclusiones eran impresionantes, la gran mayoría de pacientes estaban completamente curados de la enfermedad de Grave.
Aun así, Hertz estaba preocupado. Sintetizar yodo radiactivo en ciclotrones era un proceso tedioso, caro y muy largo; llevar a cabo estudios más grandes y aplicar los tratamientos de forma global sería complicado. Empezó a presionar a los militares para que compartieran los restos de yodo radiactivo generados durante la fabricación de bombas atómicas en Oak Ridge, Tennessee. Y lo consiguió. A partir de una bomba, diseñada para destruir vidas humanas, obtuvo el ingrediente mágico para salvarlas. Una nueva terapia prometedora.
Hertz siguió estudiando la relación entre el yodo radiactivo y la tiroides, y se convirtió en pionero de la terapia dirigida para eliminar el cáncer. Su trabajo, así como los estudios de los hermanos Lawrence, Joseph Hamilton y otros científicos, sentó las bases para el campo de la medicina nuclear. Pronto, otros descubrimientos de hombres y mujeres sucedieron a estos avances. Gracias a los conceptos de la física, la química y la medicina pudieron diseñar nuevas terapias basadas en los progresos de antes de la guerra.
En 1947 empezó a usarse yodo radiactivo para estudiar los tumores cerebrales, en 1950 para estudiar cómo se acumula la sangre en el corazón, en 1955 para estudiar el gasto cardíaco (el volumen de sangre expulsado de un ventrículo cada minuto) y para obtener imágenes del hígado. En 1982 se utilizó el yodo radiactivo para tratar melanomas malignos, una aplicación que todavía se sigue empleando. Además, se han desarrollado muchos otros radiofármacos para técnicas de imagen, diagnóstico y terapia.
Millones de pacientes (incluida la madre de Glenn Seaborg, que pudo curarse el hipertiroidismo, en parte, gracias al yodo-131 descubierto por su hijo) han disfrutado de una vida mejor gracias a los descubrimientos y colaboraciones interdisciplinares de médicos y científicos.
"Hoy, los usos médicos del yodo radiactivo siguen siendo un estándar de calidad en los tratamientos de oncología de precisión."
— "Recordando a Saul Hertz," actas del Congreso de EE.UU., 11 de mayo de 2021
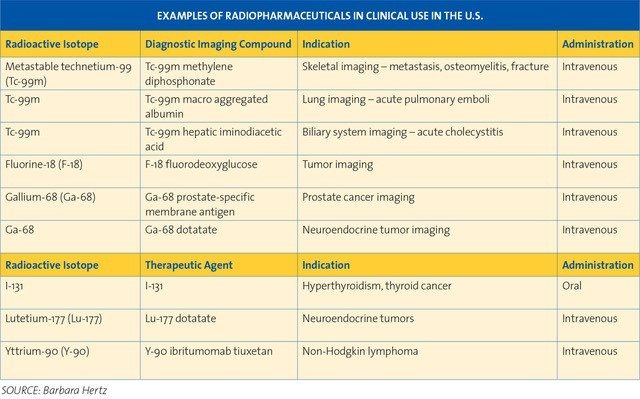
Clic para ampliar (en inglés)

Folleto en PDF (en inglés)
Dedicatoria y agradecimientos
Dedicatoria
La Sociedad Americana de Química (ACS) honró a Saul Hertz y los usos médicos del yodo radiactivo con el reconocimiento como Lugar Emblemático en la Historia de la Química (NHCL) en una ceremonia en el Hospital General de Massachusetts, en Boston, el 8 de octubre de 2021. La placa conmemorativa dice:
Poco después de que los científicos produjeran los primeros radioisótopos artificiales, el médico Saul Hertz, jefe de la clínica de tiroides del Hospital General de Massachusetts, observó que podía utilizar yodo radiactivo para tratar las enfermedades de tiroides, dado que esta glándula acumula yodo. Junto con el físico Arthur Roberts, del Instituto Tecnológico de Massachusetts, Hertz empezó a experimentar con yodo radiactivo en 1937, realizando un primer estudio con pacientes humanos del hospital el 31 de marzo de 1941. Más tarde, utilizó los mismos isótopos de yodo para tratar el cáncer. Estos avances, así como los descubrimientos de otros investigadores, sentaron las bases para la medicina nuclear. Actualmente, utilizamos yodo radiactivo (y otros radiofármacos) para diagnosticar y tratar diferentes enfermedades, para salvar y mejorar las vidas de millones de personas.
Agradecimientos
Escrito por Victoria Bruce.
La autora quiere agradecer a todos las personas que han contribuido y revisado este folleto, así como aquellos que han mejorado su contenido, especialmente los miembros del Subcomité NHCL de la ACS.
La nominación para este Lugar Emblemático fue preparada por Barbara Hertz, la Sección Noreste de la ACS, y la División de Química y Tecnología Nucleares de la ACS.
Recursos didácticos
Lecturas adicionales
- Web del doctor Saul Hertz
- “Celebrating Eighty Years of Radionuclide Therapy and the Work of Saul Hertz,” by F. H. Fahey and F. D. Grant, J. Appl. Clin. Med. Phys. 2021, 22 (1), 4–10
- “Saul Hertz, MD, and the Birth of Radionuclide Therapy,” by Frederic Fahey, Frederick Grant and James H. Thrall, EJNMMI Physics 2017, 4 (15)
- “John H. Lawrence: Nuclear Medicine Pioneer and Director of Donner Laboratory,” University of California, Berkeley, 1979, by Sally Smith Hughes
- “Donner Laboratory: Fifty Years of Nuclear Medicine Innovation,” by Karla Harby, J. Nucl. Med. 1988, 29 (4), 431-437
- “The Life and Contributions to the Periodic Table of Glenn T. Seaborg, the First Person to Have an Element Named after Him While He Was Still Alive,” by D. Seaborg, Pure Appl. Chem. 2019, 91 (12), 1929–1939
- Historical Timeline: Important Moments in the History of Nuclear Medicine, Society of Nuclear Medicine and Molecular Imaging
- “Radioactive Iodine in the Study of Thyroid Physiology. VII. The Use of Radioactive Iodine Therapy in Hyperthyroidism,” by Saul Hertz and Arthur Roberts, JAMA 1946, 131(2), 81-86
Cómo citar esta página
Lugares Emblemáticos Nacionales en la Historia de la Química, El desarrollo de la levadura química, Saul Hertz y los usos del yodo en radiomedicina (consultado el Día del Mes del Año), www.acs.org/landmarks.
Volver a la página inicial de Lugares Emblemáticos (en español)
Volver a la página inicial de Lugares Emblemáticos (en inglés)
Saber más: Sobre el programa de Lugares Emblemáticos (en inglés)
Unidades Didácticas sobre los Lugares Emblemáticos (en inglés)



