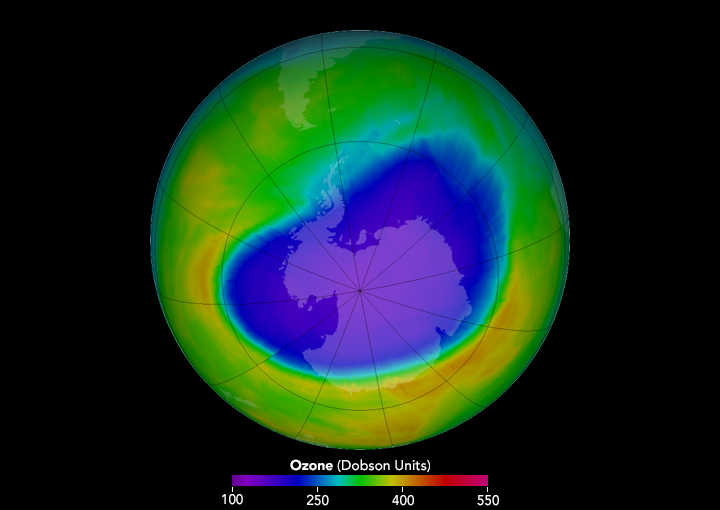
Los clorofluorocarbonos y el agujero de ozono
Otorgado en la Universidad de California, Irvine el 18 de abril de 2017.
El lenguaje es seco y académico, como corresponde al resumen de un artículo científico en la prestigiosa revista Nature. La investigación descrita en este breve artículo, sin embargo, cayó como una bomba científica cuyas repercusiones se notarían en todo el mundo. Desencadenó debates feroces, condujo a un tratado ambiental global que restringía el uso de una familia entera de sustancias químicas y cambió la forma en que los humanos veían su impacto en el medio ambiente de la Tierra. También condujo a que F. Sherwood Rowland (1927-2012) y Mario J. Molina (nacido en 1943) compartieran el Premio Nobel de Química de 1995 con Paul J. Crutzen del Instituto Max Plank de Química, Mainz (Alemania), otro pionero en la investigación del ozono estratosférico.
Rowland, profesor de química en la Universidad de California, Irvine, y Molina, becario postdoctoral en el laboratorio de Rowland, habían demostrado que los clorofluorocarbonos (CFC) podían destruir el ozono, una molécula formada por tres átomos de oxígeno (O3) en la estratosfera de la Tierra. Ese ozono estratosférico absorbe la radiación ultravioleta que, de otro modo, llegaría a la superficie de la Tierra. En ese momento, los CFC se usaban en refrigeradores, aires acondicionados y aerosoles. Estos compuestos son inertes y esencialmente no tóxicos, características que los hacen adecuados para estas aplicaciones. Sin embargo, estas mismas características también los convertían en un peligro para la vida en la Tierra.
Uso generalizado de CFC
En la década de 1920, los sistemas de refrigeración y aire acondicionado utilizaban compuestos como amoníaco, clorometano, propano y dióxido de azufre como refrigerantes. A pesar de ser eficaces, estos compuestos eran tóxicos e inflamables, y exponerse a ellos podía provocar lesiones graves, o incluso la muerte. Un equipo de químicos en Frigidaire dirigido por Thomas Midgely Jr. (1889-1944) trabajó para desarrollar alternativas no tóxicas ni inflamables a los refrigerantes.
El equipo centró sus esfuerzos en compuestos que contienen carbono y halógenos como flúor y cloro. En aquel entonces se sabía que dichos compuestos eran volátiles y químicamente inertes, propiedades ambas importantes para el equipo que estudiaba su aplicación en refrigeración. El primer compuesto que desarrollaron fue el diclorodifluorometano (CCl2F2) al que denominaron "freón". Midgely recibiría la Medalla Perkin de la Sociedad de la Industria Química por esta investigación en 1937 y, en 1941, recibió la medalla Priestley, el premio más importante de la ACS, por sus contribuciones a la química.
A principios de la década de 1970, los CFCs se habían vuelto tremendamente populares y la producción mundial de estos compuestos había alcanzado casi un millón de toneladas por año, lo que representaba aproximadamente unos 500 millones de dólares estadounidenses para la industria química.
Estamos liberando clorofluorometanos al medio ambiente en cantidades cada vez mayores. Estos compuestos son químicamente inertes, pueden permanecer en la atmósfera entre 40 y 150 años, y es esperable que sus concentraciones alcancen de 10 a 30 veces los niveles actuales. La fotodisociación de los clorofluorometanos en la estratosfera produce cantidades significativas de átomos de cloro y conduce a la destrucción del ozono atmosférico."—F. Sherwood Rowland y Mario J. Molina, Nature, 1974
La importancia del ozono
Desde un punto de vista medioambiental, el ozono es una molécula ambivalente. En la troposfera, la región baja de la atmósfera que cubre desde la superficie de la Tierra hasta poco más de nueve kilómetros y medio, el ozono es un contaminante que forma parte del smog fotoquímico. Pero en la estratosfera, la región de la atmósfera que se encuentra entre los nueve kilómetros y medio y los 50 kilómetros, el ozono absorbe la radiación ultravioleta (UV) dañina.
Tal y como lo expresó la Real Academia de Ciencias de Suecia en su anuncio del Premio Nobel de Química de 1995: “Aunque el ozono se produce en cantidades tan pequeñas, desempeña un papel excepcionalmente fundamental en la vida en la Tierra. Esto se debe a que el ozono, junto con el oxígeno molecular ordinario (O2), es capaz de absorber la mayor parte de la radiación ultravioleta del sol y, por lo tanto, evita que esta peligrosa radiación llegue a la superficie. Sin una capa protectora de ozono en la atmósfera, los animales y las plantas no podrían existir, al menos no en la tierra ".
En 1972, una conferencia despertó el interés de Rowland por el destino de los CFC en la atmósfera. El orador discutió los resultados obtenidos por James Lovelock (nacido en 1919), un científico británico que había inventado una forma altamente sensible de medir los gases presentes en cantidades traza. Lovelock había medido triclorofluorometano (CFC-11) en la atmósfera en cantidades que sugerían que prácticamente todo el CFC-11 fabricado se encontraba aún presente en la atmósfera.
Rowland decidió dedicar parte de su investigación a comprender el destino de los CFC en la atmósfera. Aunque los CFC son inertes en la troposfera inferior, se dio cuenta de que pueden ser degradados por la radiación ultravioleta una vez que se desplazan hacia la estratosfera. A fines de 1973, Rowland y Molina, quien se había unido recientemente al laboratorio de Rowland, utilizaron los datos de diversas fuentes publicadas para calcular que, a lo largo de decenas de años, las moléculas de CFC liberadas cerca de la superficie de la Tierra terminarían en la estratosfera donde la radiación UV haría que liberasen átomos de cloro. Cada átomo de cloro reaccionaría inmediatamente con una molécula de ozono, desencadenando una reacción en cadena que destruiría miles de moléculas de ozono. En su artículo, estimaron que si se prohibiera inmediatamente el uso de CFC, la pérdida de ozono continuaría durante años. Sin embargo, si continuaba la producción de CFC, la pérdida de ozono sería aún mayor.
"Cuando nos dimos cuenta de que había una reacción en cadena muy eficaz, eso cambió la investigación de CFC, que pasó de ser un problema científico que resultaba interesante a uno que tenía importantes consecuencias ambientales", dijo Rowland a Chemical & Engineering News en una extensa entrevista en 2007. "No es habitual sentir escalofríos cuando uno lee los resultados de una investigación”, agregó, pero ese había sido una de esas extrañas excepciones.
De la investigación a la resistencia
En 1976, la Academia Nacional de Ciencias de EE.UU. emitió un informe que confirmaba los efectos destructivos de los CFC sobre el ozono estratosférico. Las audiencias en el Congreso llegaron a conclusiones similares y los estados y el gobierno federal comenzaron a explorar la prohibición del uso de CFC en latas de aerosol. La industria química sostuvo que los datos sobre los CFC y el ozono estratosférico no eran concluyentes y no justificaban una acción drástica. Cuando Rowland dio una conferencia sobre los CFC, los grupos de la industria solían publicar declaraciones en las que se disputaban sus afirmaciones. Como recuerda Molina hoy, “Sherry [Rowland] era un investigador ya establecido y respetado, que solía dar charlas en todo el mundo. Parecía que, debido a su enfoque en los CFC y el desgaste del ozono, comenzó a recibir menos invitaciones a conferencias. Eso le molestó".
Rowland, Molina y el resto de científicos que intentaban comprender la química estratosférica se enfrentaron a desafíos serios y fundamentales. Un número significativo de especies químicas estaba claramente involucrado en la interacción de los CFC y el ozono en la estratosfera. La mayoría son altamente reactivos y están presentes sólo en pequeñas cantidades. Esto hacía que su química fuera difícil de replicar en el laboratorio.
Además, las concentraciones de ozono estratosférico fluctúan de forma natural, dependiendo de la geografía y la temporada. La estratosfera no es un lugar fácil de investigar. Las mediciones de la concentración de ozono se llevaron a cabo mediante instrumentos llevados a la estratosfera por globos y aviones. El ozono también se midió con instrumentos en satélites que orbitan alrededor de la Tierra, aunque la tecnología de satélites a mediados de la década de 1970 era todavía bastante primitiva.
Todas estas incertidumbres les dieron a los críticos de la hipótesis de Rowland y Molina mucho material con el que trabajar. Argumentaron, de manera muy convincente para muchos, que simplemente no tenía sentido tomar medidas contra una clase de productos químicos de gran utilidad, tomando como base una evidencia tan endeble. Los críticos de la industria, en particular, argumentaron que una cosa era proponer la eliminación progresiva del uso de CFC como propulsores en latas de aerosol, un uso relativamente trivial de los compuestos, pero otra muy distinta era considerar prohibir su uso en refrigeradores y acondicionadores de aire, cuando en ese momento no existían las alternativas directas a los CFC.
El agujero antártico de ozono
Las pruebas definitivas para respaldar la hipótesis sobre los CFC vinieron de la mano de un grupo de científicos británicos que trabajaban en la estación Halley Bay del British Antarctic Survey (BAS), donde habían estado tomando mediciones terrestres del ozono total durante décadas. En 1984, Joseph C. Farman (1930-2013) y sus colegas del BAS estudiaron los datos en bruto y encontraron que el ozono estratosférico había ido disminuyendo considerablemente desde la década de 1960. En 1985, los científicos publicaron un artículo en Nature anunciando que el ozono estratosférico sobre la Antártida se había reducido un 40% en septiembre, a finales del invierno austral.
El agujero de la capa de ozono en la Antártida convirtió el desgaste de la capa de ozono en un peligro real y urgente para los legisladores y el público en general. Las predicciones de aumentos significativos en la incidencia de cáncer de piel como resultado del uso continuo de CFC impulsaron la acción internacional. En 1987, 56 países acordaron lo que se conoció como el Protocolo de Montreal para reducir a la mitad la producción y el uso de CFC. En los años siguientes, el protocolo se reforzó para exigir una eventual eliminación mundial de la producción de CFC y otras sustancias químicas que agotan la capa de ozono.
Como resultado del trabajo de Rowland y Molina, los humanos nos dimos cuenta por primera vez de que nuestras actividades podían afectar el medio ambiente a escala planetaria. Como dijo Molina, “No importa dónde se emitan los CFC. Es un problema global. Lo importante es que condujo a un acuerdo internacional que resolvió el problema”. La saga de los CFC y la capa de ozono contiene muchas lecciones para la humanidad que se enfrenta al desafío aún mayor del cambio climático global.
Además de su trabajo, ganador del Premio Nobel, que muestra que los CFC descomponen la capa de ozono de la Tierra, Rowland y Molina fueron clave para convencer a científicos, políticos y público general de los efectos dañinos de los CFC. Su activismo sin precedentes finalmente condujo a la eliminación gradual de los CFC en todo el mundo mediante la aprobación del Protocolo de Montreal en 1987. La investigación de Rowland y Molina centró la atención de todo el mundo en el impacto de la contaminación provocada por el hombre a escala planetaria. Su trabajo fue uno de los primeros en causar de forma directa un giro global de los acontecimientos a nivel político, incluso antes del actual debate sobre el cambio climático.”—Kenneth C. Janda, profesor de química y decano, Facultad de Ciencias Físicas, Universidad de California, Irvine
Dedicación del lugar emblemático y reconocimientos
Dedicación del lugar emblemático
La ACS designó el descubrimiento de F. Sherwood Rowland y Mario J. Molina del efecto dañino de los CFC sobre el ozono como un Lugar Emblemático Nacional en la Historia de la Química en una ceremonia en la Universidad de California, Irvine, el 18 de abril de 2017. La placa conmemorativa dice:
En la Universidad de California, Irvine, F. Sherwood Rowland y Mario J. Molina descubrieron que los clorofluorocarbonos (CFC) podían agotar la capa de ozono atmosférico de la Tierra, que bloquea los dañinos rayos ultravioleta del sol. Cuando los científicos informaron sobre sus hallazgos en 1974, los CFC se usaban ampliamente como gases refrigerantes y como propulsores en aerosoles. Rowland y Molina convencieron a la industria escéptica, a los legisladores y al público del peligro de los CFC. Su activismo - y el descubrimiento por otros investigadores de que la capa de ozono sobre la Antártida se estaba adelgazando - llevó a la eliminación mundial de los CFC y al desarrollo de alternativas más seguras. Gracias a su trabajo, Rowland y Molina compartieron el Premio Nobel de Química de 1995 con otro químico atmosférico, Paul J. Crutzen.
Agradecimientos
Adaptado para Internet de "Clorofluorocarbonos y el desgaste de la capa de ozono", elaborado por el programa de lugares emblemáticos de la historia de la química de la ACS en 2017.
Recursos adicionales
Unidad Didáctica
Lecturas adicionales
- Artículo de 1974 de Molina y Rowland "Stratospheric sink for chlorofluorocarbons: chlorine atom-catalysed destruction of ozone" Nature 249 (5460), 810-812
- Mario Molina, Catedrático Distinguido de Química y Bioquímica, Univerisdad de California, San Diego
- Nota de prensa del premio Nobel de Química de 1995
- Protocolo de Montreal (a través de EPA.gov)
- Artículo de Rowland sobre cómo la investigación beneficia a la humanidad (a través de la Academia Nacional de Ciencias)
Cómo citar esta página
Lugares Emblemáticos de la Historia de la Química de la ACS. Los clorofluorocarbonos y el desgaste de la capa de ozono. http://www.acs.org/content/acs/en/education/whatischemistry/landmarks/historia-quimica/clorofluorocarbonos-ozono.html (acceso el Día de Mes de Año)
Volver a la página inicial de Lugares Emblemáticos (en español)
Volver a la página inicial de Lugares Emblemáticos (en inglés)
Saber más: Sobre el programa de Lugares Emblemáticos (en inglés)
Unidades Didácticas sobre los Lugares Emblemáticos (en inglés)